Молекул
Молекул (лат. molecula: мала маса, од лат. moles: маса), стабилна целина удружених атома. Молекул чине атоми (два или више) повезани електронима у ковалентној вези.[2][3] Молекул се може састојати од атома истих елемената (молекул елемента) на пример кисеоник у ваздуху који удишемо налази се у молекули O2.[4][5][6][7] Може се састојати и од атома различитих елемената (молекул једињења) на пример водоник (H) и кисеоник (O) граде воду H2O.
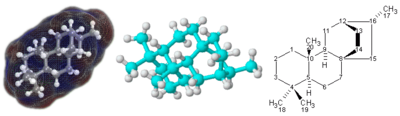
Молекули су сувише мали да би се видели голим оком. Димензија су од 0,1 до 100 нанометара (0,0000000001 до 0,00000001 m) мада има и изузетака. Рецимо макромолекул ДНК[8] а нарочито инструменталне методе.[9][10][11][12][13][14]
Однос елемената који граде једињење,[15][16] изражава се емпиријском формулом.[17] На пример, воду граде водоник и кисеоник у односу 2:1, H2O, а етил алкохол, (етанол[18]) угљеник, водоник и кисеоник у односу 2:6:1, C2H6O. Овај однос не мора увек да одређује јединствени молекул - диметил етар[19] има исти однос као етанол, на пример. Молекули који се састоје од истих атома али у различитом распореду се зову изомери.[20]
Хемијска или молекулска формула одређује тачније редослед атома који граде молекул па је формула етанола CH3CH2OH а диметилетра CH3OCH3. За представљање сложенијих молекула где атоми могу бити различито распоређени у простору користе се структурне формуле. Молекулска маса је збир маса атома који чине молекул, и попут атомске, изражава се у атомским јединицама масе (атомска јединица масе = 1/12 масе изотопа 12C).[21][22]
Дуго се мислило да су дужине хемијски веза и њихови углови у молекулу константни. Међутим, модерним структурним методама нађено је да се геометрија хемијске везе незнатно мења, нарочито код сложенијих молекула.
Наука о молекулима се назива молекулском хемијом или молекулском физиком,[23][24] у зависности од тога да ли је фокус на хемији или физици. Молекулска хемија се бави законима који владају над интеракцијама између молекула које доводе до формирања и разлагања хемијских веза, док се молекулска физика бави законима о молекулским структурама и њиховим својствима. Међутим, у пракси разлика није јасно дефинисана. У наукама о молекулима, молекул се састоји од стабилног система са два или више атома. Полиатомиски јони се могу сматрати наелектрисаним молекулима. Термин нестабилни молекул се користи за веома реактивне врсте, тј., краткотрајне констракте (резонанције) електрона и језгара, као што су радикали,[25][26] молекулски јони,[27] Ридбергови молекули,[28][29] прелазна стања,[30][31] ван дер Валсови комплекси,[32][33][34] или системи колизирајућих атома као у Бозе-Ајнштајновом кондензату.[35][36]
Историја и етимологија уреди

У Merriam-Webster речнику[39] и Онлајн етимолошком речнику,[40] реч "молекул" је изведена из латинске речи "мол" или мала јединица масе.
Молекул (1794) – „екстремно мала честица“, од фр. molécule (1678), из модерног латинског molecula, диминутива латинке речи moles „маса, баријера“. Ово наизглед непрецизно значење речи (коришћено до касног 18. века само у латинској форми) проистиче из Декартесове филозофије.[41][42]
Дефиниција молекула је еволуирала са повећањем знања о структури молекула. Ране дефиниције су биле мање прецизне, и дефинисале су молекуле као најмање честице чистих хемијских супстанци које задржавају своју композицију и хемијска својства.[43] Та дефиниција често није одржива, пошто многе супстанце, као што су стене, соли, и метали, састављене од великих кристалних мрежа хемијски везаних атома или јона, и не састоје се од засебних молекула.
Величина молекула уреди
Већина молекула је сувише мала да би се могла видети голим оком, мада постоје изузеци. ДНК макромолекул може да досегне макроскопске величине,[44][45] као и молекули многих полимера. Молекули који су уобичајени градивни блокови у органској синтези имају димензије од неколико ангстрема (Å) до неколико десетина Å. Појединачни молекули се обично не могу уочити путем обичног светла (као што је горе поменуто), али се мали молекули и чак обриси појединачних атома могу назрети у појединим околностима употребом микроскопа атомских сила.[46]
Најмањи молекулски пречник уреди
Најмањи молекул је диатомски водоник (H2), са дужином везе од 0,74 Å.[47][48]
Највећи молекулски пречник уреди
Мезопорозна силика је произведена са дијаметром од 1000 Å (100 nm)[49][50][51]
Пречник уреди
Ефективни молекулски пречник је величина који молекул има у раствору.[52][53]Табела пермселективности за разне супстанце садржи примере.[54]
Формуле молекула уреди
Типови хемијских формула уреди
Хемијска формула молекула се састоји од низа симбола хемијских елемената, бројева, а понекад и других симбола, као што су мале, средње и витичасте заграде, цртице, плус (+) и минус (−) знаци. Формуле су ограничене на појединачне типографске линије симбола, које могу да обухвате субскрипте и суперскрипте.
Емпиријска формула једињења је веома једноставни тип хемијске формуле. Она је најједноставнији целобројни однос хемијских елемената од којих се једињење састоји. На пример, вода се увек састоји од атома водоника и кисеоника у односу 2:1, а етил алкохол или етанол се увек састоји од угљеника, водоника, и кисеоника у односу 2:6:1. Међутим, то јединствено не одређује врсту молекула – на пример диметил етар има исти однос атома као етанол. Молекули са истим атомима у различитим аранжманима се називају изомерима. Такође угљени хидрати, на пример, имају исти однос (угљеник:водоник:кисеоник = 1:2:1) (и стога исту емпиријску формулу), али различите тоталне бројеве атома у молекулу.
Молекулска формула одражава прецизан број атома од којих се молекул састоји и тако карактерише различите молекуле. Различити изомери могу да имају исти атомски састав, мада су различити молекули.
Емпиријска формула је обично иста као и молекулска формула, иако то није увек случај. На пример, молекул ацетилена има молекулску формулу C2H2, док је најједноставнији целобројни однос елемената CH.
Молекулска маса се може израчунати из хемијске формуле и изражава се у конвенцијалној атомској јединици масе једнакој 1/12 масе неутралног атома угљеника-12 (12C изотопа). За умрежене чврсте материје се користи термин формула јединице у стехиометријским прорачунима.
Структурна формула уреди

За молекуле са компликованом тродимензионом структуром, посебно код молекула који садрже атоме са четири различита супституента, једноставна молекулска формула или чак полуструктурна хемијска формула, није довољна да потпуно опише молекул. У том случају се користи графички тип формуле који се назива структурном формулом.[58][58] Структурне формуле могу да се представе једнодимензионим хемијским именом, мада таква хемијска номенклатура захтева знатан број речи и чланова који нису део хемијских формула.[59][60][61]
| Структурне формуле | Остали облици | ||||||
|---|---|---|---|---|---|---|---|
| Луисова структура | Валентна формула | Ната пројекција | Скелетална формула | Конституциона формула | Молекулска формула | Емпиријска формула | |
| Метан |  |  |  | не постоји | CH4 | CH4 | CH4 |
| Пропан |  |  |  |  | CH3–CH2–CH3 | C3H8 | C3H8 |
| Сирћетна киселина |  |  |  |  | CH3–COOH | C2H4O2 | CH2O |
| Вода |  |  |  | не постоји | не постоји | H2O | H2O |
Општи просторни молекуларни модели су просторно-пуњавајући и штапићасти модел.
Геометрија молекула уреди
Молекули имају фиксне равнотежне геометрије — дужине веза и углова — око којих они непрестано осцилују путем вибрационих и ротационих кретања. Чисте супстанце се састоје од молекула са истим просечним геометријским структурама. Хемијска формула и структура молекула су два важна фактора који одређују његова својства, посебно његову реактивност. Изомери имају исту хемијску формулу али нормално имају веома различите особине услед њихових различитих структура. Стереоизомери, специфични тип изомера, могу да имају веома слична физичко-хемијска својства, а истовремено различите биохемијске активности.[62][63]
Молекулска спектроскопија уреди
Молекулска спектроскопија се бави респонсом (спектром) молекула који интерагују са тестним сигналима познате енергије (или фреквенције, у складу са Планковом формулом). Молекули имају квантизоване енергијске нивое, који се могу анализирати детектовањем молекулске енергије размене путем апсорбанције или емисије.[64]Спектроскопија се генерално не односи на дифракционе студије где честице попут неутрона, електрона, или високо енергетских X-зрака формирају интеракције са регуларним аранжманом молекула (као што је то случај са кристалима).
Теоретски аспекти уреди
Изучавање молекула у молекулској физици и теоретској хемији је углавном базирано на квантној механици и есенцијално је за разумевање хемијске везе. Најједноставнији молекул је водонични молекулски јон, H2+, и најједноставнија од свих хемијских веза је једноелектронска веза. H2+ се састоји од два позитивно наелектрисана протона и једног негативно наелектрисаног електрона, што значи да се Шредингерова једначина система може лакше решити услед недостатка електрон–електрон репулзије. Са развојем брзих дигиталних рачунара, приближна решења за компликованије молекуле су постала могућа и један су од главних аспеката рачунарске хемије.[65][66][67]
У покушају да ригорозно дефинише аранжман атома који је довољно стабилан да би се сматрао молекулом, IUPAC сугерише да он мора да одговара „удубљењу на површини потенцијалне енергије које је довољно дубоко да ограничи бар једно вибрационо стање“.[4] Ова дефиниција није зависна од природе интеракције између атома, него само од јачине интеракције. Заправо, она обухвата само слабо везане врсте аранжмана који се традиционално не би сматрали молекулима, као што су хелијумски димер, He2, који има једно вибрационо везано стање[68] и у тој мери је лабаво везан да се једино може уочити на веома ниским температурама.
Да ли је или не аранжман атома „довољно стабилан“ да би се сматрао молекулом је инхерентно операциона дефиниција. Филозофски, стога, молекул није фундаментални ентитет (у контрасту, на пример са елементарном честицом[69]); већ је концепт молекула хемичарски начин прављења корисних изјава о јачини интеракција на атомској скали.
Види још уреди
- Атом
- Ван дер Валсов молекул
- Диатомски молекул
- Геометрија молекула
- Мали молекул
- Ефузија, врста протока гасних молекула
- Хемијска поларност
- Молекулска геометрија
- Ковалентна веза
- Нековалентно везивање
- Молекуларни Хамилтонијан
- Молекуларни јон
- Молекулска орбитала
- Молекулско моделовање
- Софтвер за молекулски дизајн
- Периодни систем малих молекула
Референце уреди
Литература уреди
- Karplus, Martin; Porter, Richard N. (1970). Atoms and Molecules: An Introduction for Students of Physical Chemistry. Benjamin & Company, Inc. ISBN 9780805352184.
- Frenkel, Daan; Smit, Berend (1996). Understanding Molecular Simulation: From Algorithms to Applications. Academic Press. ISBN 978-0-12-267370-2.
- A.R. Leach (2001). Molecular Modelling: Principles and Applications. Prentice Hall. ISBN 978-0-582-38210-7.
- Choppin, G.; Liljenzin, J. O.; Rydberg, J. (1995). Radiochemistry and Nuclear Chemistry (2nd изд.). Butterworth-Heinemann. стр. 3–5. ISBN 9780750623001.
- Eliel, Samuel; Ernest L. H. Wilen (1994). Stereochemistry of Organic Compounds. Wiley Interscience. стр. 52–53. ISBN 9780471016700.
- Petrucci R.H.; Harwood R.S.; Herring F.G. (2002). General Chemistry (8th изд.). Prentice-Hall. стр. 91.
- Compendium of Terminology and Nomenclature of Properties in Clinical Laboratory Sciences. IMPACT Recommendations 1995. Oxford: Blackwell Science. 1995. ISBN 978-0-86542-612-2.
- Nomenclature of Organic Chemistry (3rd изд.). London: Butterworths. 1971 [1958 (A: Hydrocarbons, and B: Fundamental Heterocyclic Systems), 1965 (C: Characteristic Groups)]. ISBN 978-0-408-70144-0.
- Boron, Walter F.; Boulpaep, Emile L. (2005). Medical Physiology: A Cellular And Molecular Approach. Elsevier/Saunders. стр. 761. ISBN 978-1-4160-2328-9.
- DeKock, Roger L.; Gray, Harry B.; Gray, Harry B. (1989). Chemical structure and bonding. University Science Books. стр. 199. ISBN 978-0-935702-61-3.
- Hammond, C.R. (2012). „Section 4: Properties of the Elements and Inorganic Compounds”. Handbook of Chemistry and Physics (PDF). Архивирано из оригинала (PDF) 11. 11. 2011. г. Приступљено 14. 02. 2017.
- Reif, F. (1965). Fundamentals of Statistical and Thermal Physics (International student изд.). Boston: McGraw-Hill. стр. 2. ISBN 978-0-07-051800-1. „we shall call a system "macroscopic" (i.e., "large scale") when it is large enough to be visible in the ordinary sense (say greater than 1 micron, so that it can at least be observed with a microscope using ordinary light).”
- Russell, Bertrand (1946). History of Western Philosophy. Psychology Press. стр. 516. ISBN 978-0-415-32505-9.
- Shankar, R. (1994). Principles of Quantum Mechanics (2nd изд.). Kluwer Academic/Plenum Publishers. стр. 143. ISBN 978-0-306-44790-7.
- Smith, R. Angus (1856). Memoir of John Dalton and History of the Atomic Theory. London: H. Bailliere. стр. 279. ISBN 978-1-4021-6437-8. Приступљено 24. 12. 2007.
- Brown, T. L.; Kemp, Kenneth C.; Brown, Theodore L.; LeMay, Harold Eugene; Bursten, Bruce Edward (2003). Chemistry – the Central Science (9th изд.). New Jersey: Prentice Hall. ISBN 978-0-13-066997-1.
- Ebbin, Darrell D. (1990). General Chemistry (3rd изд.). Boston: Houghton Mifflin Co. ISBN 978-0-395-43302-7.
- Miessler, Gary L.; Tarr, Donald Arthur (2004). Inorganic chemistry. Prentice Hall. ISBN 978-0-13-035471-6.
- Solomons, T.W. Graham; Fryhle, Craig B. (2004). Organic Chemistry (8th изд.). John Wiley & Sons, Inc. ISBN 978-0-471-41799-6.
- Mount, DM (2004). Bioinformatics: Sequence and Genome Analysis (2 изд.). Cold Spring Harbor, NY: Cold Spring Harbor Laboratory Press. ISBN 978-0-87969-712-9. OCLC 55106399.
- Firn, Richard (2010). Nature's Chemicals. Oxford: Biology.
- Miessler, Gary L.; Tarr, Donald Arthur (2004). Inorganic chemistry. Prentice Hall. ISBN 978-0-13-035471-6.
- March, Jerry (1992). Advanced organic chemistry: reactions, mechanisms, and structure. John Wiley & Sons. ISBN 978-0-471-60180-7.
- Brown, T.L. (2003). Chemistry – the Central Science (9th изд.). New Jersey: Prentice Hall. ISBN 978-0-13-066997-1.
- Chang, Raymond (1998). Chemistry (6th изд.). New York: McGraw Hill. ISBN 978-0-07-115221-1.
- Ebbin, Darrell, D. (1990). General Chemistry (3rd изд.). Boston: Houghton Mifflin Co. ISBN 978-0-395-43302-7.
- Nieman, Timothy A.; Skoog, Douglas A.; Holler, F. James (1998). Principles of instrumental analysis. Pacific Grove, CA: Brooks/Cole. ISBN 978-0-03-002078-0.
- Puling, Linus (1970). General Chemistry. New York: Dover Publications, Inc. ISBN 978-0-486-65622-9.
- Pauling, Linus (1970). General Chemistry. New York: Dover Publications, Inc. ISBN 978-0-486-65622-9.
- Zumdahl, Steven S. (1997). Chemistry (4th изд.). Boston: Houghton Mifflin. ISBN 978-0-669-41794-4.
- Татевский, Владимир Михайлович Квантовая механика и теория строения молекул. — М.: Изд-во МГУ, 1965. — 162 с.
- Бейдер, Ричард Атомы в молекулах. Квантовая теория. — М.: Мир, — 532 c. 2001. ISBN 978-5-03-003363-1.
- Минкин, Владимир Исаакович, Симкин Б. Я., Миняев Р. М. Теория строения молекул. — М.: Высшая школа, 1979. — 408 с.
- Кук Д., Квантовая теория молекулярных систем. Единый подход. Пер с англ. М.: Интеллект, — 256с. 2012. ISBN 978-5-91559-096-9.
Спољашње везе уреди
- Наука 50: Молекул (РТС Образовно-научни прогам - Званични канал)
- Molecule of the Month – School of Chemistry, University of Bristol
- Молекулы (видеурок, программа 7 класса)
- Molecule // IUPAC Gold Book
- Molecular entity // IUPAC Gold Book
- Молекула: Сайт о Химии
- Шредингер Э. Волновая теория механики атомов и молекул. УФН 1927
- Статья «Молекула» в Физической энциклопедии



