글리옥실산
글리옥실산(영어: glyoxylic acid) 또는 옥소아세트산(영어: oxoacetic acid)은 유기 화합물이다. 아세트산, 글리콜산, 옥살산과 함께 글리옥실산은 C2 카복실산의 한 종류이다. 글리옥실산은 자연에서 생성되는 무색 고체로 산업적으로 유용하다.
 | |
 | |
| 이름 | |
|---|---|
| 우선명 (PIN) oxoacetic acid[1] | |
| 체계명 oxoethanoic acid | |
| 별칭 | |
| 식별자 | |
3D 모델 (JSmol) | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.005.508 |
| KEGG | |
PubChem CID | |
| UNII | |
CompTox Dashboard (EPA) | |
| |
| |
| 성질 | |
| C2H2O3 | |
| 몰 질량 | 74.035 g·mol−1 |
| 밀도 | 1.384 g/mL |
| 녹는점 | 80 °C (176 °F; 353 K)[4] |
| 끓는점 | 111 °C (232 °F; 384 K) |
| 산성도 (pKa) | 3.18,[2] 3.32[3] |
| 관련 화합물 | |
다른 음이온 | 글리옥실레이트 |
관련 카복실산 | 폼산 아세트산 글리콜산 옥살산 프로피온산 피루브산 |
관련 화합물 | 아세트알데하이드 글리옥살 글리콜알데하이드 |
달리 명시된 경우를 제외하면, 표준상태(25 °C [77 °F], 100 kPa)에서 물질의 정보가 제공됨. | |
구조 및 명명법 편집
글리옥실산의 구조는 카보닐기(알데하이드 작용기)를 가지고 있는 것으로 설명되지만, 알데하이드는 일부 상황에서 널리 퍼진 형태의 일부 성분일 뿐이다. 대신 글리옥실산은 종종 수화물 또는 고리형 이량체로 존재한다. 예를 들어 물이 있을 때 카보닐기는 제미날 다이올("일수화물"로 설명됨)로 빠르게 전환된다. 평형 상수(K)는 실온에서 다이하이드록시 아세트산의 형성에 대해서는 300이다.[5]
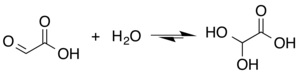 |
용액에서 일수화물은 헤미아세탈 이량체 형태와 평형 상태로 존재한다.[6]
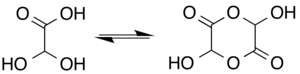 |
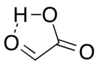
분리되었을 때 알데하이드 구조는 카복실 수소에 매우 근접한 알데하이드 카보닐과 함께 고리형 수소 결합 구조를 주요 형태이성질체로 가지고 있다.[7]
 |
글리옥실산의 헨리의 법칙 상수는 KH = 1.09 × 104 × exp[(40.0 × 103/R) × (1/T − 1/298)]이다.[8]
제조 편집
글리옥실산의 짝염기는 글리옥실레이트(영어: glyoxylate)로 알려져 있으며, 화합물이 중성 pH에서 용액에 존재하는 형태이다. 글리옥실레이트는 여러 아마이드화된 펩타이드의 생합성에서 아마이드화 과정의 부산물이다.
과거에 글리옥실산은 옥살산으로부터 전기합성적으로 제조되었다.[9][10] 유기 합성에서 황산 전해질에서 옥살산으로부터 글리옥실산을 제조하기 위해 이산화 납 음극을 사용하였다.[11]
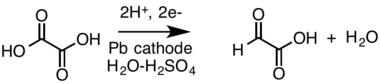 |
뜨거운 질산은 글리옥살을 글리옥실로 산화시킬 수 있다. 그러나 이 반응은 발열성이 크고 열 폭주가 일어나기 쉬우며 옥살산은 주요 부산물이다.
생물학적 역할 편집
글리옥실산은 글리옥실산 회로의 대사 중간생성물로 글리옥실산 회로는 세균,[12]균류, 식물[13]과 같은 생물이 지방산을 탄수화물로 전환할 수 있도록 한다. 글리옥실산 회로는 균류에 대한 식물의 방어 기작의 유도에도 중요하다.[14] 글리옥실산 회로는 아이소시트르산을 글리옥실산과 석신산으로 전환시키는 아이소시트르산 분해효소의 활성을 통해 시작된다. 석신산 생합성과 같은 다양한 용도로 경로를 선택하기 위한 연구가 진행되고 있다.[15]
사람에서 편집
글리옥실산은 크게 두 가지 경로를 통해 생성되는 데, 하나는 퍼옥시좀에서 글리콜산의 산화를 통해 생성되고 다른 하나는 미토콘드리아에서 하이드록시프롤린의 이화대사를 통해 생성된다.[16] 퍼옥시좀에서 글리옥실산은 AGT1에 의해 글리신으로 전환되거나 글리콜산 산화효소에 의해 옥살산으로 전환된다. 소량의 글리옥실산은 세포질의 젖산 탈수소효소에 의해 옥살산으로 전환된다.[17]
 |
식물에서 편집
글리옥실산은 글리옥실산 회로의 대사 중간생성물일 뿐만 아니라 광호흡 경로의 중요한 대사 중간생성물이기도 하다. 광호흡은 루비스코가 CO2 대신 O2와 반응할 때 일어난다. 광호흡은 처음에는 에너지와 자원의 낭비인 것으로 간주되었지만, 이후의 연구에 따르면 광호흡은 탄소와 CO2를 재생성하고, 독성을 가지는 포스포글리콜산을 제거하여 방어 메커니즘을 작동시키는 중요한 역할을 하는 것으로 밝혀졌다.[18][19] 광호흡에서 글리옥실산은 퍼옥시좀에서 글리콜산 산화효소의 활성을 통해 글리콜산으로부터 생성된다. 그런 다음 SGAT와 GGAT의 작용을 통해 글리신으로 전환된 다음 미토콘드리아로 운반된다.[20][19] 또한 피루브산 탈수소효소 복합체가 글리콜산 및 글리옥실산 대사에 역할을 할 수 있다고 보고되었다.[21]
질병과의 관련성 편집
당뇨병 편집
글리옥실산은 제2형 당뇨병에 대한 잠재적인 초기 마커로 생각된다.[22] 당뇨병 병리의 주요 조건들 중 하나는 고혈당증으로 인한 최종 당화 산물의 생성이다.[23] 최종 당화 산물은 조직 손상 및 심혈관계 질환과 같은 당뇨병의 추가적인 합병증을 유발시킬 수 있다.[24] 이들은 일반적으로 환원당 및 알파-옥소알데하이드에 존재하는 것과 같은 반응성 알데하이드로부터 형성된다. 한 연구에서 글리옥실산의 수치는 나중에 제2형 당뇨병 진단을 받은 환자에서 유의미하게 증가하는 것으로 나타났다.[22] 상승된 수치는 진단전 최대 3년 전에 발견되어 글리옥실산이 조기 예측 마커가 될 수 있는 잠재성을 보여준다.
신장결석증 편집
글리옥실산은 신장결석증(일반적으로 신장결석으로 알려져 있음)의 주요 원인인 고옥살산뇨의 발생에 관여한다. 글리옥실산은 옥살산 수송을 담당하는 유전자인 설페이트 음이온 수송체-1(sulfate anion transporter-1, sat-1)의 기질이자 유도 물질이며, 이를 통해 sat-1 mRNA 발현을 증가시키고 결과적으로 세포로부터 옥살산의 유출을 증가시킬 수 있다. 증가된 옥살산의 방출은 소변에 칼슘 옥살레이트를 축적시켜서 결국에 신장결석을 생성시킨다.[17]
글리옥실산의 대사 교란은 고옥살산뇨증 발병의 추가적인 메커니즘을 제공한다. HOGA1 유전자의 돌연변이는 하이드록시프롤린에서 글리옥실산 경로로의 효소인 4-하이드록시-2-옥소글루타르산 알돌레이스의 손실로 이어진다. 이 경로에서 생성된 글리옥실산은 일반적으로 세포질에서 옥살산으로의 산화를 방지하기 위해 다른 먼 곳에 저장된다. 그러나 교란된 경로는 4-하이드록시-2-옥소글루타르산의 축적을 유발하며, 이는 또한 세포질로 수송될 수 있고 다른 알돌레이스를 통해 글리옥실산으로 전환될 수 있다. 이러한 글리옥실산 분자는 옥살산으로 산화되어 옥살산의 농도를 증가시키고 고옥살산뇨증을 유발할 수 있다.[16]
반응 및 용도 편집
글리옥실산은 아세트산보다 약 10배 정도 더 강한 산이며, 산 해리상수는 4.7 × 10−4 (pKa = 3.32)이다.
- OCHCO2H ⇄ OCHCO−
2 + H+
염기와 있으면 글리옥실산은 불균등화되어 하이드록시아세트산과 옥살산을 형성한다.
- 2 OCHCO2H + H2O → HOCH2CO2H + HO2CCO2H
글리옥실산은 요소 및 1,2-다이아미노벤젠과의 축합으로 헤테로고리를 생성한다.
페놀 유도체 편집
일반적으로 글리옥실산은 페놀과 친전자성 방향족 치환 반응을 하며, 이 반응은 여러 다른 화합물의 합성에서 다양하게 사용된다.
페놀 자체가 있는 중간생성물은 4-하이드록시만델산이다. 4-하이드록시만델산은 암모니아와 반응하여 아목시실린의 전구체인 하이드록시페닐글리신을 생성한다. 4-하이드록시만델산의 환원은 아테놀올의 전구체인 4-하이드록시페닐아세트산을 생성한다.
글리옥실산이 페놀 성분인 구아야콜과 반응한 후 산화 및 탈카복실화되는 일련의 반응은 순 폼일화 과정으로 바닐린에 대한 경로를 제공한다.[6][25][26]
홉킨스-콜 반응 편집
글리옥실산은 단백질에서 트립토판의 존재를 확인하는 데 사용되는 홉킨스-콜 반응의 구성 요소이다.[27]
환경화학 편집
글리옥실산은 2차 유기 에어로졸과 함께 풍부한 케톤 및 알데하이드 함유 카복실산들 중 하나이다. 물과 햇빛이 있는 곳에서 글리옥실산은 광화학 산화를 겪을 수 있다. 여러 가지 다른 반응들이 이어질 수 있으며 다양한 다른 카복실산 및 알데하이드 생성물이 만들어진다.[28]
안전 편집
글리옥실산은 쥐에서 2500 mg/kg의 반수 치사량으로 독성이 거의 없다.
각주 편집
- ↑ 가 나 〈Front Matter〉. 《Nomenclature of Organic Chemistry : IUPAC Recommendations and Preferred Names 2013 (Blue Book)》. Cambridge: The Royal Society of Chemistry. 2014. 748쪽. doi:10.1039/9781849733069-FP001. ISBN 978-0-85404-182-4.
- ↑ Dissociation Constants Of Organic Acids and Bases (600 compounds), http://zirchrom.com/organic.htm.
- ↑ pKa Data Compiled by R. Williams, “Archived copy” (PDF). 2010년 6월 2일에 원본 문서 (PDF)에서 보존된 문서. 2010년 6월 2일에 확인함..
- ↑ Merck Index, 11th Edition, 4394
- ↑ Sørensen, P. E.; Bruhn, K.; Lindeløv, F. (1974). “Kinetics and equilibria for the reversible hydration of the aldehyde group in glyoxylic acid.”. 《Acta Chem. Scand.》 28: 162–168. doi:10.3891/acta.chem.scand.28a-0162.
- ↑ 가 나 다 Georges Mattioda and Yani Christidis “Glyoxylic Acid” Ullmann's Encyclopedia of Industrial Chemistry, 2002, Wiley-VCH, Weinheim. doi 10.1002/14356007.a12_495
- ↑ Redington, Richard L.; Liang, Chin-Kang Jim (1984). “Vibrational spectra of glyoxylic acid monomers”. 《Journal of Molecular Spectroscopy》 104 (1): 25–39. Bibcode:1984JMoSp.104...25R. doi:10.1016/0022-2852(84)90242-X.
- ↑ Ip, H. S. Simon; Huang, X. H. Hilda; Yu, Jian Zhen (2009). “Effective Henry's law constants of glyoxal, glyoxylic acid, and glycolic acid” (PDF). 《Geophysical Research Letters》 36 (1): L01802. Bibcode:2009GeoRL..36.1802I. doi:10.1029/2008GL036212.
- ↑ Tafel, Julius; Friedrichs, Gustav (1904). “Elektrolytische Reduction von Carbonsäuren und Carbonsäureestern in schwefelsaurer Lösung”. 《Berichte der Deutschen Chemischen Gesellschaft》 37 (3): 3187–3191. doi:10.1002/cber.190403703116.
- ↑ Cohen, Julius (1920). 《Practical Organic Chemistry 2nd Ed.》 (PDF). London: Macmillan and Co. Limited. 102–104쪽.
- ↑ François Cardarelli (2008). 《Materials Handbook: A Concise Desktop Reference》. Springer. 574쪽. ISBN 978-1-84628-668-1.
- ↑ Holms WH (1987). “Control of flux through the citric acid cycle and the glyoxylate bypass in Escherichia coli”. 《Biochem Soc Symp.》 54: 17–31. PMID 3332993.
- ↑ Escher CL, Widmer F (1997). “Lipid mobilization and gluconeogenesis in plants: do glyoxylate cycle enzyme activities constitute a real cycle? A hypothesis”. 《Biol. Chem.》 378 (8): 803–813. PMID 9377475.
- ↑ Dubey, Mukesh K.; Broberg, Anders; Sooriyaarachchi, Sanjeewani; Ubhayasekera, Wimal; Jensen, Dan Funck; Karlsson, Magnus (September 2013). “The glyoxylate cycle is involved in pleotropic phenotypes, antagonism and induction of plant defence responses in the fungal biocontrol agent Trichoderma atroviride”. 《Fungal Genetics and Biology》. 58–59: 33–41. doi:10.1016/j.fgb.2013.06.008. ISSN 1087-1845. PMID 23850601.
- ↑ Zhu, Li-Wen; Li, Xiao-Hong; Zhang, Lei; Li, Hong-Mei; Liu, Jian-Hua; Yuan, Zhan-Peng; Chen, Tao; Tang, Ya-Jie (November 2013). “Activation of glyoxylate pathway without the activation of its related gene in succinate-producing engineered Escherichia coli”. 《Metabolic Engineering》 20: 9–19. doi:10.1016/j.ymben.2013.07.004. ISSN 1096-7176. PMID 23876414.
- ↑ 가 나 Belostotsky, Ruth; Pitt, James Jonathon; Frishberg, Yaacov (2012년 12월 1일). “Primary hyperoxaluria type III—a model for studying perturbations in glyoxylate metabolism”. 《Journal of Molecular Medicine》 90 (12): 1497–1504. doi:10.1007/s00109-012-0930-z. hdl:11343/220107. ISSN 0946-2716. PMID 22729392. S2CID 11549218.
- ↑ 가 나 Schnedler, Nina; Burckhardt, Gerhard; Burckhardt, Birgitta C. (March 2011). “Glyoxylate is a substrate of the sulfate-oxalate exchanger, sat-1, and increases its expression in HepG2 cells”. 《Journal of Hepatology》 54 (3): 513–520. doi:10.1016/j.jhep.2010.07.036. ISSN 0168-8278. PMID 21093948.
- ↑ “photorespiration”. 2006년 12월 11일에 원본 문서에서 보존된 문서. 2017년 3월 9일에 확인함.
- ↑ 가 나 Peterhansel, Christoph; Horst, Ina; Niessen, Markus; Blume, Christian; Kebeish, Rashad; Kürkcüoglu, Sophia; Kreuzaler, Fritz (2010년 3월 23일). “Photorespiration”. 《The Arabidopsis Book / American Society of Plant Biologists》 8: e0130. doi:10.1199/tab.0130. ISSN 1543-8120. PMC 3244903. PMID 22303256.
- ↑ Zhang, Zhisheng; Mao, Xingxue; Ou, Juanying; Ye, Nenghui; Zhang, Jianhua; Peng, Xinxiang (January 2015). “Distinct photorespiratory reactions are preferentially catalyzed by glutamate:glyoxylate and serine:glyoxylate aminotransferases in rice”. 《Journal of Photochemistry and Photobiology B: Biology》 142: 110–117. doi:10.1016/j.jphotobiol.2014.11.009. ISSN 1011-1344. PMID 25528301.
- ↑ Blume, Christian; Behrens, Christof; Eubel, Holger; Braun, Hans-Peter; Peterhansel, Christoph (November 2013). “A possible role for the chloroplast pyruvate dehydrogenase complex in plant glycolate and glyoxylate metabolism”. 《Phytochemistry》 95: 168–176. doi:10.1016/j.phytochem.2013.07.009. ISSN 0031-9422. PMID 23916564.
- ↑ 가 나 Nikiforova, Victoria J.; Giesbertz, Pieter; Wiemer, Jan; Bethan, Bianca; Looser, Ralf; Liebenberg, Volker; Ruiz Noppinger, Patricia; Daniel, Hannelore; Rein, Dietrich (2014). “Glyoxylate, a New Marker Metabolite of Type 2 Diabetes”. 《Journal of Diabetes Research》 2014: 685204. doi:10.1155/2014/685204. ISSN 2314-6745. PMC 4265698. PMID 25525609.
- ↑ Nguyen, Dung V.; Shaw, Lynn C.; Grant, Maria B. (2012년 12월 21일). “Inflammation in the pathogenesis of microvascular complications in diabetes”. 《Frontiers in Endocrinology》 3: 170. doi:10.3389/fendo.2012.00170. ISSN 1664-2392. PMC 3527746. PMID 23267348.
- ↑ Piarulli, Francesco; Sartore, Giovanni; Lapolla, Annunziata (April 2013). “Glyco-oxidation and cardiovascular complications in type 2 diabetes: a clinical update”. 《Acta Diabetologica》 50 (2): 101–110. doi:10.1007/s00592-012-0412-3. ISSN 0940-5429. PMC 3634985. PMID 22763581.
- ↑ Fatiadi, Alexander; Schaffer, Robert (1974). “An Improved Procedure for Synthesis of DL-4-Hydroxy-3-methoxymandelic Acid (DL-"Vanillyl"-mandelic Acid, VMA)”. 《Journal of Research of the National Bureau of Standards Section A》 78A (3): 411–412. doi:10.6028/jres.078A.024. PMID 32189791.
- ↑ Kamlet, Jonas; Mathieson, Olin (1953). 《Manufacture of vanillin and its homologues U.S. Patent 2,640,083》 (PDF). U.S. Patent Office.
- ↑ R.A. Joshi (2006). 《Question Bank of Biochemistry》. New Age International. 64쪽. ISBN 978-81-224-1736-4.
- ↑ Eugene, Alexis J.; Xia, Sha-Sha; Guzman, Marcelo I. (2016). “Aqueous Photochemistry of Glyoxylic Acid”. 《J. Phys. Chem. A》 120 (21): 3817–3826. Bibcode:2016JPCA..120.3817E. doi:10.1021/acs.jpca.6b00225. PMID 27192089.
