Šarlah
Šarlah (lat. scarlatina) je zarazna bolest koja nastaje kao posledica infekcije sojem piogenog streptokaka (Streptococcus pyogenes) koji luči neku od izoformi streptokoknog pirogenog egzotoksina (SPE A, B ili C). U toku 18. i početkom 19. veka šarlah je bio teška, pa i smrtonosna bolest, ali, usled, za sada neobjašnjenog, pada virulencije uzročnog mikroorganizma u tridesetim godinama 20. veka, kao i zbog moderne terapije, to je sada, uglavnom, laka dečija bolest.[1]
| Šarlah | |
|---|---|
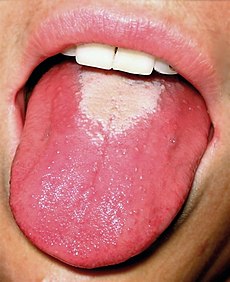 | |
| Jezik pacijenta sa šarlahom | |
| Specijalnost | Infectious disease |
| Klasifikacija i eksterni resursi | |
| ICD-10 | A38 |
| ICD-9 | 034.1 |
| DiseasesDB | 29032 |


uredi
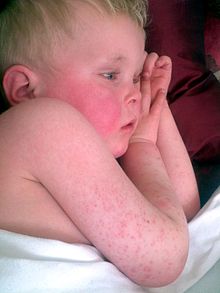
Šarlah je akutna zarazna bolest iz grupe streptokokoza. Bolest počinje naglo, sa znacima temperature, gušobolje i pojavom sitne, zrnkaste makulopapularne ospe na koži i sluzokoži. Ospa može biti praćena tačkastim krvarenjima, koja su uočljiva na mestima pregiba, kao što su vrat, lakat, prepone i struk. Ospe na licu nema. Iščezavanje ospe praćeno je perutanjem kože, karakterističnom pojavom za šarlah.
Ukoliko se bolest ne leči na vreme, kao komplikacija može nastati zapaljenje velikih zglobova i srčanog mišića, poznato pod imenom reumatska groznica. Dijagnoza ovog oboljenja postavlja sa na osnovu epidemiološke ankete, karakteristične zrnaste ospe i nalaza infektivnog agensa u brisu ždrela.
Infektivni agens uredi
Infektivni agens je bakterija Streptococcus pyogenes, koja ima preko osamdeset različitih tipova. Sposobnost lučenja eritrogenog toksina, odgovornost za pojavu ospe kod šarlaha, značajna je za ovu bakteriju.
Streptococcus pyogenes je otporan u spoljašnjoj sredini, a u biološkom materijalu, na primer ispljuvku, može se održati nekoliko nedelja.
Inkubacioni period uredi
Kod šarlaha inkubacioni period kratak, 1 — 3 dana, a nekada može biti i duži.
Rezervoar zaraze uredi
Rezervoar zaraze su bolesnik od šarlaha i kliconoša. Zaraznost zavisi od vremena primenjene terapije. Ukoliko se lečenje primeni odmah, zaraznost se skraćuje na jedan do dva dana. Suprotno, zaraznost je duga i traje obično deset dana kod bolesnika. Kod kliconoša zaraznost traje do tri nedelje.
Put prenosa uredi
Bolest se širi Fligeovim kapljicama i poljupcem.
Ulazno mesto uredi
Ulazno mesto je sluzokoža gornjih disajnih puteva.
Osetljivost i otpornost uredi
Osetljivost je opšta. Posle preležane bolesti antitoksična otpornost obično je trajna.
Ostale epidemiološke karakteristike uredi
Šarlah se endemski javlja u gradovima, a epidemije bolesti se registruju u dečjim kolektilivima, naručito u školama. Sezona porasta obolevanja je jesenje-zimski period godine, koji se poklapa i sa formiranjem dečjih kolektiva, odnosno sa polaskom u školu. U tim situacijama boravak u zatvorenom prostoru i blizak kontakt obezbeđuju širenje šarlaha Fligelovim kapljicama.
Mere sprečavanja uredi
Primena higijenskih uslova rada i života u dečjim kolektivima može sprečiti pojavu bolesti. Provetravanje prostoriaj kolektivnog boravka u predškolskim ustanovama, školama i internatima i otkrivanje kliconoša Streptococcusa pyogenesa u njima osnovne su mere sprečavanja bolesti.
Mere suzbijanja uredi
Šarlah se suzbija obaveznom prijavom, ranim otkrivanjem bolesnika i primenom izolacije i lečenja. U odnosu na kolektiv, kod lica iz kontakta sa bolesnikom otkrivaju se kliconoše infektivnog agensa.
Patofiziologija uredi
Šarlah se obično širi putem vazduha (udisanjem), mada se može preneti dodirom ili kohabitacijom. Mada se normalno ne smatra bolešću koja se prenosi hranom, poznato je da je došlo do epidemije šarlaha izazvane infektiranim piletinom u Kini.[2]
Asimptomatsko prenošenje se može javiti kod 15–20% dece školskog uzrasta.
Inkubacioni period je 1–4 dana.
Mikrobiologija uredi
Sama bolest je uzrokovana sekrecijom pirogenih eksotoksina iz infekcionih Streptococcus bakterija.[3][4] Eksotoksin A (speA) je verovatno najbolje izučen među tim toksinima. On se prenosi putem Bakteriofaga T12 koji se integriše u streptokokalni genom, odakle se toksin transkribuje. Sam fag se integriše u gen serinske tRNK na hromozomu.[5]
Međunarodni komitet za taksonomiju virusa ne stavlja sam T12 virus u takson. Virus ima dvolančani DNK genom i sa morfološkog stanovišta smatra se članom Siphoviridae.
Gen speA je kloniran i sekvenciran 1986 godine.[6] On sadrži 753 baznih parova i kodira protein sa 29.244 kilo Daltona (kDa). Protein sadrži pretpostavljeni 30 aminokiselina dug signalni peptid. Uklanjanje signalne sekvence daje predviđenu molekulsku težinu od 25,787 (kDa) izlučenog proteina. Promoter i mesto vezivanja ribozoma (Shine-Dalgarno sekvenca) se nalaze ispred gene. Terminator transkriptije je lociran 69 baza niže od kodona translacione terminacije. Karboksilno terminalni deo proteina je ekstenzivno homologan sa karboksilnim terminusom Staphylococcus aureus enterotoksina B i C1.
Drugi streptokokalni fagovi, pored T12, mogu da nose speA gen.[7]
Panton-Valentinski leukocidin uredi
Panton–Valentinski leukocidin (PVL) je dvokomponentni citotoksin čija meta su ljudski i zečiji neutrofili, monociti i makrofazi.[8] Manje od 5% vrsta Staphylococcus aureus koje imaju PVL gen, proizvode ovaj toksin kao faktor virulencije, i odgovorne su za infekcije kože i pneumoniju,[9] i asocirane su sa društeveno stečenom meticilinskom otpornošću.[10][11] PVL je povezan sa pogoršanim manifestacijama kože i inflamatornim responsom kod dece sa stafilokokalnim šarlahom.[12]
Reference uredi
- ↑ Edward J Zabawski Jr. „Scarlet Fever”. MedScape Reference.
- ↑ Yang, S. G.; Dong, H. J.; Li, F. R.; Xie, S. Y.; Cao, H. C.; Xia, S. C.; Yu, Z.; Li, L. J. (2007). „Report and analysis of a scarlet fever outbreak among adults through food-borne transmission in China”. Journal of Infection 55 (5): 419–424. DOI:10.1016/j.jinf.2007.07.011. PMID 17719644.
- ↑ Zabriskie, J. B. (1964). „The role of temperate bacteriophage in the production of erythrogenic toxin by Group A Streptococci”. Journal of Experimental Medicine 119 (5): 761–780. DOI:10.1084/jem.119.5.761. PMC 2137738. PMID 14157029.
- ↑ Krause, R. M. (2002). „A Half-century of Streptococcal Research: Then & Now”. Indian Journal of Medical Research 115: 215–241. PMID 12440194.
- ↑ McShan, W. M.; Ferretti, J. J. (1997). „Genetic diversity in temperate bacteriophages of Streptococcus pyogenes: identification of a second attachment site for phages carrying the erythrogenic toxin A gene”. J Bacteriol 179 (20): 6509–6511. PMC 179571. PMID 9335304.
- ↑ Weeks, C. R.; Ferretti, J. J. (1986). „Nucleotide sequence of the type A streptococcal exotoxin (erythrogenic toxin) gene from Streptococcus pyogenes bacteriophage T12”. Infect Immun 52 (1): 144–150. PMID 262210.
- ↑ Yu, C. E.; Ferretti, J. J. (1991). „Molecular characterization of new group A streptococcal bacteriophages containing the gene for streptococcal erythrogenic toxin A (speA)”. Mol Gen Genet 231 (1): 161–168. DOI:10.1007/BF00293833. PMID 1753942.
- ↑ Prévost, G; Mourey, L; Colin, DA; Menestrina, G (2001). „Staphylococcal pore-forming toxins.”. Current topics in microbiology and immunology 257: 53–83. DOI:10.1007/978-3-642-56508-3_4. PMID 11417122.
- ↑ Lina, G.; Piemont, Y.; Godail-Gamot, F.; Bes, M.; Peter, M.-O.; Gauduchon, V.; Vandenesch, F.; Etienne, J. (1 November 1999). „Involvement of Panton–Valentine Leukocidin—Producing Staphylococcus aureus in Primary Skin Infections and Pneumonia”. Clinical Infectious Diseases 29 (5): 1128–1132. DOI:10.1086/313461. PMID 10524952.
- ↑ Voyich, Jovanka M .; Otto, Michael; Mathema, Barun; Braughton, Kevin R.; Whitney, Adeline R.; Welty, Diane; Long, R. Daniel; Dorward, David W. i dr.. (15 December 2006). „Is Panton-Valentine Leukocidin the Major Virulence Determinant in Community-Associated Methicillin-Resistant Disease?”. The Journal of Infectious Diseases 194 (12): 1761–1770. DOI:10.1086/509506. PMID 17109350.
- ↑ Vandenesch, F; Naimi, T; Enright, MC; Lina, G; Nimmo, GR; Heffernan, H; Liassine, N; Bes, M i dr.. (August 2003). „Community-acquired methicillin-resistant Staphylococcus aureus carrying Panton-Valentine leukocidin genes: worldwide emergence.”. Emerging Infectious Diseases 9 (8): 978–84. DOI:10.3201/eid0908.030089. ISSN 1080-6040. PMC 3020611. PMID 12967497.
- ↑ Lo, Wen-Tsung; Tang, Ching-Shen; Chen, Shyi-Jou; Huang, Ching-Feng; Tseng, Min-Hua; Wang, Chih-Chien (1 October 2009). „Panton‐Valentine Leukocidin Is Associated with Exacerbated Skin Manifestations and Inflammatory Response in Children with Community-Associated Staphylococcal Scarlet Fever”. Clinical Infectious Diseases 49 (7): e69–e75. DOI:10.1086/605580. PMID 19725782.
Literatura uredi
- Rolleston JD (November 1928). „The history of scarlet fever”. British Medical Journal 2 (3542): 926–9. DOI:10.1136/bmj.2.3542.926. PMC 2456687. PMID 20774279.
- D. F. Erhard: Ueber die äußerliche Anwendung des kalten Wassers als Heilmittel im Scharlachfieber. Beck, Nördlingen 1824 (Digitalisierte Ausgabe der Universitäts- und Landesbibliothek Düsseldorf)
Vanjske veze uredi
- Scarlet Fever from PubMed Health
- Scharlach
- Scharlach im eMedicine
